对于大多数人来说,金属是铁,钢或类似的硬质物质的另一个词。
但这个定义是否适合金属的真实特性?
是的......而且没有。
在我们解释之前,您应该知道大多数元素周期表是金属。
金属在周期表的中心和左侧发现。它们可以进一步分类为碱金属,碱土金属,过渡金属和基本金属。
金属科学教训
金属的性质
一个元素是由一种物质组成的物质原子;它不能分成更简单的部件。例如,元素氦(思考热气球)专门由氦原子组成。
元素通常被归类为金属要么非金属(尽管一些元素具有两者的特征;这些都被称为金属化)。
金属的三种性质是:
- 光泽:在切割,划伤或抛光时,金属闪亮。
- 延展性:金属坚固但可延展,这意味着它们可以容易地弯曲或形状。几个世纪以来,史密斯已经能够通过加热金属和用锤子捣碎来塑造金属物体。如果他们用非金属试过这个,那么物质会破碎!大多数金属也是如此韧性,这意味着它们可以被抽出来制造电线。
- 电导率:金属是电力和热量的优异导体。因为它们也是韧性,所以它们是电气布线的理想选择。(您可以使用一些家庭物品测试这一点。继续阅读以了解如何!)
额外的金属属性
高熔点:大多数金属具有高熔点,除汞外的所有金属在室温下都是固体。
铿son:金属经常在击中时发出响铃声。
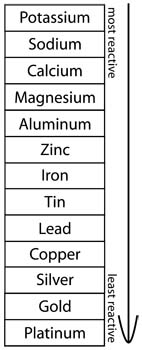
反应性:一些金属将经历化学变化(反应),自身或其他元素,并释放能量。这些金属从未以纯形式发现,并且难以与所发现的矿物分开。钾和钠是最活力的金属。它们与空气和水剧烈反应;钾会点燃与水的接触!
其他金属与其他金属无关。这意味着它们可以以纯形式发现(例子是金和铂)。因为铜相对便宜且具有低的反应性,因此对制造管道和布线是有用的。
五组金属:
贵金属被发现为纯金属,因为它们是不反应的并且与其他元素不相结合以形成化合物。因为它们是如此不反应,所以他们不易腐蚀。这使它们成为珠宝和硬币的理想选择。贵金属包括铜,钯,银,铂和金。
碱金属是非常有反应的。它们具有低熔点,并且足够柔软地用刀切切割。钾和钠是两种碱金属。
碱土金属在具有许多不同矿物质的化合物中发现。它们与碱金属的反应较小,以及更稠固,并且具有更高的熔点。该组包括钙,镁和钡。
过渡金属我们在想到金属时通常会想到什么。它们是艰难而有光泽的,强壮的,易于塑造。它们用于许多工业目的。该组包括铁,金,银,铬,镍和铜,其中一些也是惰性金属。
金属差是相当柔软的,大多数人自己都没有用。但是,当添加到其他物质时,它们变得非常有用。差金属包括铝,镓,锡,铊,锑和铋。
合金:强大的组合
这些不同金属的性质可以通过将两个或更多个混合在一起来组合。所得物质称为合金。我们最有用的建筑材料实际上是合金。例如,钢是铁和少量碳和其他元素的混合物;一种强大且易于使用的组合。(加入铬,你得到不锈钢。检查你的厨房锅和平底锅,看看有多少由不锈钢制成!)
其他合金如黄铜(铜和锌)和青铜(铜和锡)易于塑造和美观。青铜器也经常在船舶建设中使用,因为它是抵抗海水的腐蚀。
钛比钢更轻,更密集,但坚强;虽然比铝更重,但它也是两倍的强烈。它也耐腐蚀性也很耐受。所有这些因素使其成为优异的合金材料。钛合金用于飞机,船舶和航天器,以及涂料,自行车,甚至是笔记本电脑!
作为纯金属的金色是如此柔软,即在它的珠宝制成时,它总是与另一种金属(通常是银,铜或锌)混合。金的纯度测量karats.。最纯粹的你可以进入珠宝是24个karats,大约是99.7%的纯金。金也可以与其他金属混合以改变其颜色;白金是珠宝流行的,是金和铂或钯的合金。
来自矿石的金属
矿石是岩石或矿物质可以提取有价值的物质 - 通常是金属 - 可以提取。一些常见的矿石包括Galena(铅矿),凤蝶和孔雀石(铜),朱砂(汞)和铝土矿(铝)。最常见的铁矿石是磁铁矿和赤铁矿(由铁和氧形成的生锈型矿物),其含有约70%的铁。
有几个过程精制矿石的铁。较旧的方法是用波纹管提供的木炭(碳)和氧气燃烧铁矿石。碳和氧气,包括矿石中的氧气,结合并离开铁。然而,铁不足以完全融化,它含有留在矿石上留下的硅酸盐。它可以加热并敲打形成锻铁。
更现代的过程使用高炉加热铁矿石,石灰石和焦炭(煤制品,而不是软饮料)。所得反应将铁从矿石中的氧气分离出来。这种“猪铁”需要进一步混合以产生锻铁。它还可以用于另一种重要的目的:用碳和其他元素加热时,它变成了更强的金属钢。
考虑到所涉及的过程,它并不令人惊讶于铁被使用直到1500年大约在1500年到1500左右。但之前使用了一些纯金属 - 金,银和铜,并被认为已经被苏美尔人在3500年左右发现了合金青铜。但铝是现代使用中最重要的金属之一,并未发现到公元1825年,并在20世纪之前没有常用!
腐蚀:过程和预防
你有没有见过一块偏离它的银色,或者用腐蚀引起的红麦锈的铁,甚至是漏洞的铁?这发生在氧气(通常来自空气)与金属反应时发生。具有较高反应性的金属(如镁,铝,铁,锌和锡)更容易发生这种化学破坏,或者腐蚀。

当氧气与金属反应时,它形成一个氧化物在金属表面上。在一些金属,如铝,这是一件好事。氧化物提供一种保护层,该保护层将金属保持进一步腐蚀。
另一方面,钢铁,如果没有治疗以防止腐蚀,则具有严重问题。在铁或钢上形成时的红色氧化物层被称为氧气锈。锈层不断剥落,将更多金属暴露于腐蚀直至金属最终通过。
保护铁的一种常用方法是用特殊涂料涂抹,使氧气与涂料下面的金属反应。另一种方法是镀锌:在这个过程中,钢涂有锌。空气中的氧气,水分子和二氧化碳与锌反应,形成保护免受腐蚀的碳酸锌层。环顾房屋,院子和车库,腐蚀的例子以及镀锌和保护金属的镀锌手段。
技术:烟花与化学
如果您在7月的第四次观看烟花,您将看到美丽的颜色组合和火花。
这款惊人的烟火展出工作如何?短暂的答案是化学。较长的涉及金属的性质的回顾。
鞭炮,地面烟花和空中烟花(在天空中爆炸的空中烟花(天空)的关键成分之一是黑火药,由大约1000年前的中国人发明。它是硝酸钾(盐渗漏),木炭和硫的混合物,75:15:10比率。黑色粉末用于发射天线,并导致特殊效果如噪声或彩色光所需的爆炸。
在烟火中,黑色粉末与金属粉末和其他化合物的形式混合,其将缓慢地燃烧,顶部到底部。在简单的烟火火箭中,黑色粉末被限制在保险丝周围的管中。点亮时,粉末产生导致的力平等和反应,将烟火从地面推,然后使其内部的化合物在空中爆炸。
更复杂的烟火壳由砂浆发射,带有黑色粉末的管,引起灯光时的剥离反应。然后,烟花壳的保险丝随着它进入空气,并且在壳体内部爆炸导致其特殊效果收取爆发。

烟花显示的明亮彩色部分是由不同金属和盐化合物原子中的“激发”电子引起的。这些化合物叫做小球星星,由类似的化合物制成,以使烟火作用。
金属作为着色剂
不同的金属燃烧不同的颜色;例如,如果铜化合物点亮,其火焰将是蓝绿色。钙烧红色和钾烧伤紫色。在烟花中,金属组合以产生不同的颜色。
当烟花内的星形化合物被加热时,兴奋原子会产生光能。这盏灯分为两类:白炽和发光。白炽是从热量产生的光线:在烟花中,铝和镁等反应金属会导致当它们变热时爆裂非常明亮的光 - 有时在5000°F超过5000°F的温度下!
无反应性的化合物不会变热,导致调光火花。发光另一方面,由其他来源产生,即使在寒冷的温度下也可以发生。复合中的电子吸收能量,使它们“兴奋”。然而,电子不能保持这种高电平,因此它们跳到较低水平,在该过程中释放光能(光子)。
氯化钡是一种化合物,使烟花发光绿色,氯化铜产生蓝色。对于任何一种光,重要的是使用纯成分,因为其他化合物的痕迹将遮挡颜色。






